研究概要:診断・治療へ応用可能なマイクロ流体デバイスの開発
臨床検体に含まれるバイオマーカー(病気の兆候や特徴を示す分子)を高速・高感度・低コスト・低侵襲に検出する技術を開発し、「どこでも診断」「個別化医療」「精密医療」といった次世代医療技術を実現することが研究の目的です。最近はデバイスの社会実装を目指して、
- IoTやマイクロコンピュータを用いた「だれでも簡単に使えるマイクロ流体デバイス用自動分析システム」の開発
- 持続可能な社会の実現と次世代医療の両立を目的とした医療デバイス向け新規材料の開発
なども行っています。
これまでの研究1:非小細胞肺がんに対する分子標的薬の効果を予測
がんの代表的な分子標的薬である上皮成長因子受容体(EGFR)チロシンキナーゼ阻害薬は、肺がんの80%を占める非小細胞肺がんのドライバー遺伝子変異として最も患者数が多い遺伝子変異(L858R型とexon 19欠損型)に対して著効することが知られており、日本肺癌学会ガイドラインにおいて、薬剤投与前に腫瘍細胞の遺伝子変異型診断を行うよう推奨されている。しかしこの診断は、病院外の臨床検査機関で実施され、1週間のターンアラウンドタイムを要する。また、1検体の分析費用は約2万円であり、医療費増大の原因にもなっている。本研究は、迅速・低コストで極微量検体の分析が可能なマイクロ流路デバイスによって免疫学的に遺伝子変異型EGFRを検出し、これらの問題を解決することを目的として進められた。
これまでの研究で、L858R型とexon 19欠損型の遺伝子変異EGFR高感度診断デバイスを作製し、0.25 μLという微量の肺がん患者の胸水から、短時間(20分)かつ高感度(従来法の10倍)に、1分析あたり200円という低コストで、前処理なしに遺伝子変異型EGFRを特異的に検出することに成功している。
発表論文・書籍など
- 医の希望 (岩波新書、齋藤 英彦 (編集))
- T. Kasama, Y. Baba, and M. Tokeshi, Next generation point-of-care biomedical sensors technologies for cancer diagnosis (Springer, Singapore, 2017), pp. 305-322.
- 小野島 大介, 笠間 敏博, 馬場嘉信: がん診断に向けたラボオンチップの実用化, CSJカレントレビュー第24号「医療・診断・創薬の化学 医療分野に挑む革新的な科学技術」(化学同人), 78-83, 2017.
- T. Kasama, N. Kaji, M. Tokeshi, and Y. Baba, Microchip diagnostics (Springer-Verlag GmbH, 2017), pp. 49-56.
- N. Yogo, T. Hase, T. Kasama, K. Nishiyama, N. Ozawa, T. Hatta, H. Shibata, M. Sato, K. Komeda, N. Kawabe, K. Matsuoka, T.F. Chen-Yoshikawa, N. Kaji, M. Tokeshi, Y. Baba, and Y. Hasegawa, PLOS ONE 15, e0241422 (2020). doi: 10.1371/journal.pone.0241422.
- N. Yogo, T. Hase, T. Kasama, T. Hatta, N. Ozawa, M. Sato, N. Kaji, M. Tokeshi, Y. Baba, Y. Hasegawa, Development of the immuno-wall device for rapid detection of ALK and ROS1 fusions in lung cancer, Annals of Oncology. 29 (2018) ix120. (IF: 18.3)
- N. Yogo, T. Hase, T. Kasama, N. Ozawa, M. Sato, N. Kaji, M. Tokeshi, Y. Baba, and Y. Hasegawa, Annals of Oncology 28, X118 (2017). (IF: 18.3)
主な学会発表
- 與語 直之, 長谷 哲成, 笠間 敏博, 八田 貴広, 小沢 直也, 佐藤 光夫, 馬場 嘉信, 長谷川 好規, 肺癌における迅速なEGFR・ALK・ROS1遺伝子検査を目的としたマイクロ免疫診断チップ開発, 第116回日本内科学会総会・講演会, 名古屋市, 2019/4/28
- 笠間 敏博, イムノアッセイによる遺伝子変異型タンパク質の特異的検出と、精密医療への応用, 分析化学会, 仙台市, 2018/9/12, Invited
- 笠間 敏博, イムノウォールデバイスによるタンパク質分析と脳腫瘍診断および肺がんコンパニオン診断への応用, 名古屋大学グリーン自然科学国際教育研究プログラムIGERシンポジウム, 名古屋市, 2016/12/16, Invited
- “Development of rapid and low-cost detection method for EGFR mutations in cytological samples from patients with Non-small cell lung cancer”, T. Hase, T. Kasama, N. Nishiwaki, N. Yogo, M. Sato, N. Kaji, M. Kondo, M. Tokeshi, Y. Baba and Y. Hasegawa, 16th World Conference on Lung Cancer, 2015.9.6-9.9, Denver, USA
- “Rapid and Low-Cost Detection of Mutant Epidermal Growth Factor Receptors from Cytological Samples in Lung Cancer Patients – Development of New Companion Diagnostics Devices”, T. Kasama, T. Hase, N. Nishiwaki, N. Yogo, M. Sato, M. Kondo, N. Kaji, M. Tokeshi, Y. Hasegawa and Y. Baba, MicroTAS 2015, 2015.10.25-10.29, Gyeongju, South Korea(採択率約60%)
これまでの研究2:脳腫瘍と正常脳の境界の術中鑑別と、脳腫瘍患者の予後を術中に予測
脳に浸潤した状態で存在する脳腫瘍を外科手術により完全に摘出することは、正常脳を傷つける恐れがあることから非常に困難である。残存した脳腫瘍は、やがて再発し、死に至る。しかし、脳腫瘍に特異的かつ広範に認められるタンパク質であるR132H変異型イソクエン酸デヒドロゲナーゼ1(IDH1)を摘出した組織から術中に検出できれば、正常脳と腫瘍の境界を厳密に調べることができるため、手術の精度を大きく向上できると考えられる。また、R132H変異型IDH1による低グレードグリオーマは予後がよいことが報告されており、術中検査が可能になれば、手術の方針決定にも有用である。本研究は、切除した数mm程度の脳腫瘍の中のR132H変異型IDH1を迅速に分析可能なマイクロ流路デバイスを開発することを目的として進められた。
これまでの研究で、溶解した脳腫瘍を分析し、迅速に遺伝子変異型IDH1を検出することに成功している。分析に要した時間は約9分であり、術中にも十分に実行可能である。本研究の成果により、脳腫瘍の外科手術の高精度化と脳腫瘍患者の生存率の向上が期待される。
発表論文・書籍など
- T. Kasama, Y. Baba, and M. Tokeshi, Next generation point-of-care biomedical sensors technologies for cancer diagnosis (Springer, Singapore, 2017), pp. 305-322.
- 小野島 大介, 笠間 敏博, 馬場嘉信: がん診断に向けたラボオンチップの実用化, CSJカレントレビュー第24号「医療・診断・創薬の化学 医療分野に挑む革新的な科学技術」(化学同人), 78-83, 2017.
- T. Kasama, N. Kaji, M. Tokeshi, and Y. Baba, Microchip diagnostics (Springer-Verlag GmbH, 2017), pp. 49-56.
- A. Yamamichi, T. Kasama, F. Ohka, H. Suzuki, A. Kato, K. Motomura, M. Hirano, M. Ranjit, L. Chalise, M. Kurimoto, G. Kondo, K. Aoki, N. Kaji, M. Tokeshi, T. Matsubara, T. Senga, M.K. Kaneko, H. Suzuki, M. Hara, T. Wakabayashi, Y. Baba, Y. Kato, and A. Natsume, Science and Technology of Advanced Materials 17, 618 (2016).
- Toshihiro Kasama, Akane Yamamichi, Fumiharu Ohka, Yukinari Kato, Hiromichi Suzuki, Akira Kato, Kazuya Motomura, Masanori Hirano, Melissa Ranjit, Lushun Chalise, Michihiro Kurimoto, Goro Kondo, Kosuke Aoki, Noritada Kaji, Toshio Matsubara, Hidenori Suzuki, Manabu Tokeshi, Toshihiko Wakabayashi, Atsushi Natsume and Yoshinobu Baba, IMMUNO-WALL LAB-ON-A-CHIP PROTEIN ANALYSIS DEVICES FOR HIGH PRECISION SURGERY OF GLIOMAS, microTAS 2016.
主な学会発表
- Kasama Toshihiro, Intraoperative ultra-high speed genotyping of brain tumors by using microfluidic immunoassay devices, The 3 rd International Symposium on Biomedical Engineering, Hiroshima, Japan, 2018/11/10, Invited
- 笠間 敏博, イムノアッセイによる遺伝子変異型タンパク質の特異的検出と、精密医療への応用, 分析化学会, 仙台市, 2018/9/12, Invited
- 夏目 敦至, 山道 茜, 大岡 史治, 鈴木 啓道, 青木 恒介, 笠間 敏博, 若林 俊彦, 加藤 幸成, 馬場 嘉信, 分子夾雑に基づく脳腫瘍細胞解析と脳腫瘍分子診断, 日本化学会, 川崎市, 2017/3/16, Invited
- Toshihiro Kasama, Akane Yamamichi, Fumiharu Ohka, Yukinari Kato, Hiromichi Suzuki, Akira Kato, Kazuya Motomura, Masanori Hirano, Melissa Ranjit, Lushun Chalise, Michihiro Kurimoto, Goro Kondo, Kosuke Aoki, Noritada Kaji, Toshio Matsubara, Hidenori Suzuki, Manabu Tokeshi, Toshihiko Wakabayashi, Atsushi Natsume and Yoshinobu Baba, IMMUNO-WALL LAB-ON-A-CHIP PROTEIN ANALYSIS DEVICES FOR HIGH PRECISION SURGERY OF GLIOMAS, microTAS 2016.(採択率約60%)
- 笠間 敏博, イムノウォールデバイスによるタンパク質分析と脳腫瘍診断および肺がんコンパニオン診断への応用, 名古屋大学グリーン自然科学国際教育研究プログラムIGERシンポジウム, 名古屋市, 2016/12/16, Invited
- 笠間 敏博, 山道 茜, 大岡 史治, 加藤 幸成, 加藤 彰, 平野 雅規, Lushun Chalise, 栗本 路弘, 近藤 五郎, 青木 恒介, 鈴木 啓道, 本村 和也, 加地 範匡, 渡慶次 学, 松原 年生, 鈴木 秀鎌, 若林 俊彦, 夏目 敦至, 馬場 嘉信, 脳腫瘍の完全切除を目指した術中遺伝子変異診断, 化学とマイクロ・ナノシステム学会, 千葉市, 2016/9/7
これまでの研究3:紙ベースのマイクロ分析チップ ~液体流れの制御と検出技術~
自動分析装置は、その高い分析精度や自動化性能のおかげで、医用診断には欠かせない装置となっている。一方、マイクロ加工技術を利用して作成するマイクロ分析チップが、全体を小型化でき、使い捨てでの利用が期待できることから、上記装置を補完する、あるいは代替する装置技術として注目されている。現状、このマイクロ分析チップの基材としては、プラスチック、シリコンエラストマーなどが使われているが、使い捨てにする場合、依然として材料コストの点で課題がある。これに対して、近年、マイクロ分析チップの基材として「紙」が盛んに取り上げられるようになっている。「紙」は極めて安価な材料であり、かつ焼却性に優れているため無害化にも有利である。
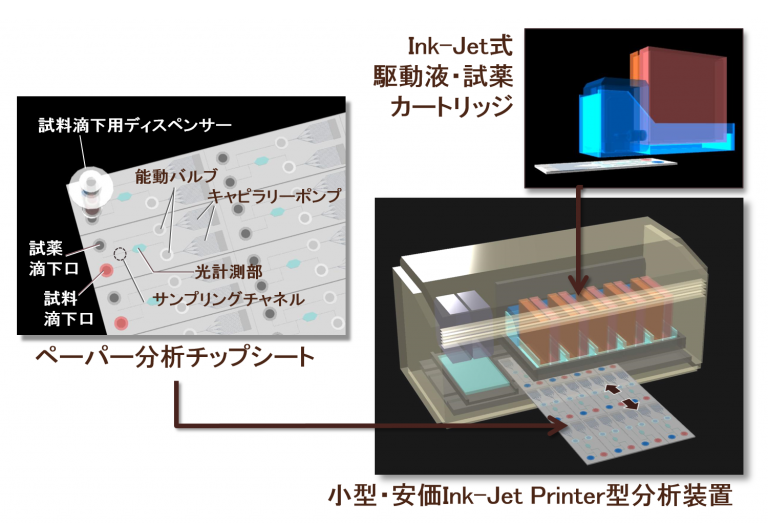 上に紙ベースの分析チップをシート状にした概念図、インクジェットプリンタを模した自動分析装置の概念図を示す。技術課題として、①紙基材上に精度の良い流路を作製する加工技術、②駆動液の滴下をきっかけとして液体の流れを開始・制御する技術、さらに③試薬反応による変化を紙面上で検出する技術等を新たに開発する必要がある。上記の課題を受けて、①マイクロチップの作成技術、②チップ上での液体の流れを開始・制御する技術、③試薬反応による変化を紙面上で検出する技術の開発を行っている。
上に紙ベースの分析チップをシート状にした概念図、インクジェットプリンタを模した自動分析装置の概念図を示す。技術課題として、①紙基材上に精度の良い流路を作製する加工技術、②駆動液の滴下をきっかけとして液体の流れを開始・制御する技術、さらに③試薬反応による変化を紙面上で検出する技術等を新たに開発する必要がある。上記の課題を受けて、①マイクロチップの作成技術、②チップ上での液体の流れを開始・制御する技術、③試薬反応による変化を紙面上で検出する技術の開発を行っている。

紙ベースマイクロ分析チップ |

試作装置外観 |
